
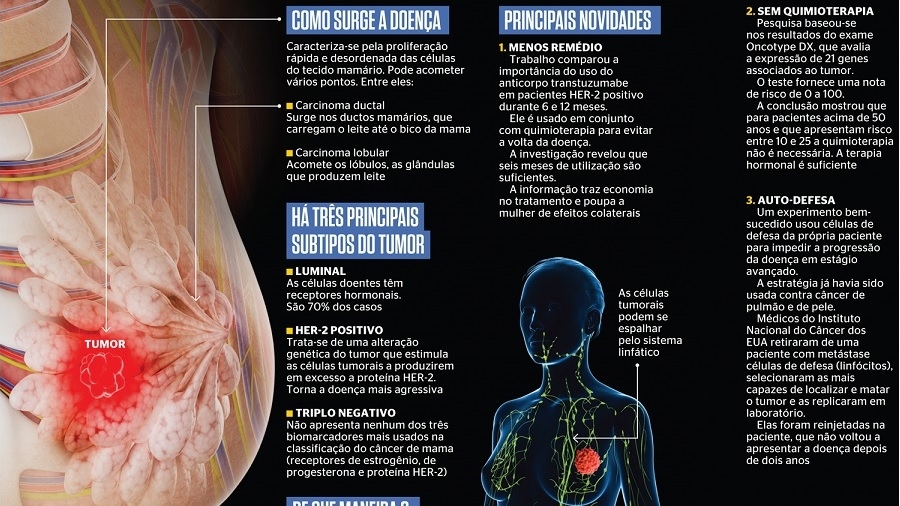
O medicamento Tecentriq® (Atezolizumabe), indicado como monoterapia para tratamento de câncer de pulmão não pequenas células (CPNPC) e carcinoma urotelial (UC), ambos localmente avançados ou metastáticos, teve um novo risco identificado à sua utilização: a miosite imunorrelacionada, inflamação nos músculos que pode causar a degeneração dos tecidos progressivamente.
Recomenda-se que o tratamento com Tecentriq® (Atezolizumabe) seja suspenso em casos de miosite imunorrelacionada moderada ou severa (Graus 2 ou 3) e que seja permanentemente descontinuado em casos de miosite recorrente severa ou potencialmente fatal (Graus 3 e 4 recorrentes). Nesses casos, é necessário encaminhar o paciente a um reumatologista e/ou neurologista, considerar a realização da biópsia muscular e adotar medidas de suporte, caso indicado. O tratamento com o corticosteroide metilpredinisolona na dose de 1-2 mg/Kg/dia por via intravenosa, ou em uma dose mais elevada em bolus, deve ser considerado em casos de comprometimento severo (fraqueza limitando severamente a mobilidade, funções cardíaca e respiratória, e disfagia). O uso de agentes imunossupressores deve ser administrado caso ocorram eventos de Grau 2 ou superiores ou se o evento não melhorar após corticosteroides iniciais.
A Roche informou que o texto de bula de Tecentriq® (Atezolizumabe) será atualizado, a fim de refletir o risco de miosite imunorrelacionada, de acordo com as regulamentações aplicáveis. Após aprovação da ANVISA, a bula estará disponível para consulta nos canais apropriados da Roche e da própria ANVISA. Com vistas a minimizar esse risco, é recomendado que os profissionais de saúde sigam as orientações de manejo descritas acima. O perfil de benefício-risco de Tecentriq® (Atezolizumabe) nas indicações aprovadas permanece favorável. Para acessar a bula atual de Tecentriq® (atezolizumabe), clique aqui.
Notificações
Os profissionais de saúde devem reportar quaisquer suspeitas de eventos adversos com Tecentriq® (Atezolizumabe) por meio do sistema eletrônico para a notificações relacionadas ao uso de medicamentos da ANVISA (VigiMed) ou diretamente para a Roche:[email protected] / [email protected] / 0800-77-20-292.
Veja o comunicado da Roche na íntegra – clique aqui.






















































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































Endereço
Avenida Paulista, 2073, Edifício Horsa II – Conjunto Nacional Conj. 1003, São Paulo/SP, 01311-300
Telefone
+55 (11) 3192-9284