

Em meio à pandemia de COVID-19 e da urgência por respostas científicas para seu enfrentamento, a Sociedade Brasileira de Oncologia Clínica (SBOC) enviou carta aos deputados federais em que reforça sua defesa pela aprovação do projeto de lei 7.082/2017, que regulamenta e acelera o andamento de estudos clínicos com potencial para melhorar a vida de pacientes oncológicos e da população em geral.
Em tramitação na Comissão de Constituição, Justiça e Cidadania na Câmara dos Deputados (CCJC), o PL é de autoria da ex-senadora Ana Amélia Lemos, subscrito também pelos ex-senadores Waldemir Moka e Valter Pinheiro, e teve início no Senado em 2015, com o projeto de lei suplementar 200. Desde então, a iniciativa vem sendo discutida e aprimorada até chegar ao texto atual, que, se aprovado, define o Marco Regulatório da Pesquisa Clínica no Brasil.
De acordo com Dra. Ana Gelatti, da Diretoria SBOC e coordenadora do Comitê de Pesquisa Clínica da entidade, o marco trará uma regulamentação adequada para a pesquisa clínica no Brasil, proporcionando maior agilidade com qualidade e garantias de segurança e valores éticos para o cuidado com os pacientes. “O país só tem a ganhar com chegada de novos incentivos na área da pesquisa, como qualificação dos nossos profissionais, estímulo para desenvolvimento local de novos estudos, agilidade nos processos e, principalmente, credibilidade internacional”, acredita. “Dessa forma, teremos maior arsenal para que as decisões sejam baseadas em evidências, e não em opiniões.”
Avanços
Entre os benefícios que o Marco Regulatório trará à pesquisa clínica brasileira está uma maior autonomia às decisões da Comissão Nacional de Ética em Pesquisa (CONEP), protegendo os critérios técnico-científicos que devem orientá-las, como é de praxe em comissões de análises de bioéticas ao redor do mundo.
“Nos últimos meses, com a chegada do novo coronavírus, assuntos que pouco eram discutidos voltaram à tona. Novas medicações e vacinas, como realizar estudos clínicos, qual o nível científico de cada um, tudo isso ganhou os holofotes não apenas da área da saúde, mas também da população em geral, que, diante da gravidade da situação, preocupa-se com a necessidade de encontrarmos opções de tratamento e cuidado”, explica Dra. Ana Gelatti.
Para ela, “é de extrema importância que todo esse diálogo seja pautado pelo conhecimento científico, e o Marco Regulatório oferece garantias para que respostas científicas sejam alcançadas”.
A iniciativa também desburocratiza o início das pesquisas. Entre as medidas com esse fim está a garantia da aprovação dos protocolos de pesquisa em instância única, diferente do que ocorre hoje, quando cada protocolo de cooperação internacional precisa ser aprovado em um comitê de ética na instituição onde será executado. Depois, todos precisam ser avaliados novamente pela CONEP. “Uma redundância desnecessária e que só existe no Brasil”, reforça Dr. Fábio André Franke, também do Comitê de Pesquisa Clínica da SBOC.
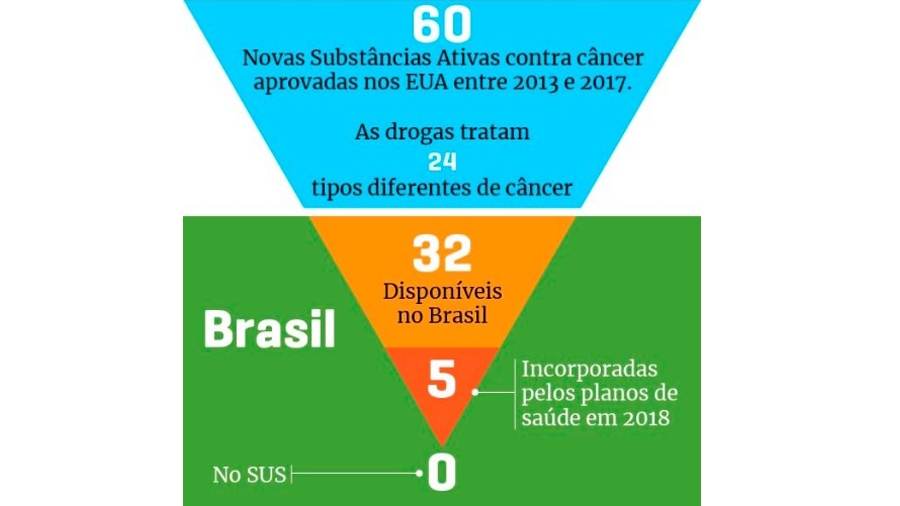
Para Dr. Gustavo Girotto, que também integra o comitê, o PL beneficia em especial os pacientes oncológicos. “Trata-se de um texto maduro que traz todos os players e organizações de pesquisa para uma discussão com condições para melhorar dramaticamente a pesquisa clínica nacional, atraindo mais protocolos e tecnologia para oferecer à população sem que as garantias éticas sem menosprezadas. Estamos perdendo oportunidades a cada dia, especialmente para os brasileiros com câncer, dado o dinamismo dos avanços da oncologia internacional. Isso permitirá que eles recebam os melhores cuidados e possam viver mais e melhor.”
Além disso, o Marco Regulatório garante que todos os participantes de pesquisa clínica, ao final da sua participação no estudo, tenham direito a continuar recebendo a medicação experimental, desde que estejam obtendo benefício e se enquadrem nos requisitos da lei. “Isso traz segurança jurídica e transparência para os pacientes e pesquisadores”, reforça Dr. Gustavo Girotto.
Para Dra. Ana Gelatti, a pandemia de COVID-19 torna ainda mais urgente a aprovação do Marco Regulatório. “A SBOC acredita que esse seja um dos momentos mais propícios para alertarmos nossos governantes sobre a importância e o impacto que teremos em âmbito nacional com a aprovação do PL 7.082/2017”, reforça. “Para quem trabalha há anos com pesquisa clínica é emocionante ver o envolvimento de um grande número de profissionais na tentativa de desenvolver estudos locais e em busca de melhores desfechos para nossos pacientes. A população se viu frente a uma urgência científica, e nós, profissionais, da saúde tivemos a oportunidade de expor as dificuldades e os entraves por trás da aprovação de novas drogas e tecnologias.”
O PL aguarda pelo parecer do relator na Comissão de Constituição e Justiça e de Cidadania (CCJC) da Câmara. Leia a íntegra da carta enviada pela SBOC aos deputados.

















































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































































Endereço
Avenida Paulista, 2073, Edifício Horsa II – Conjunto Nacional Conj. 1003, São Paulo/SP, 01311-300
Telefone
+55 (11) 3192-9284